國家獸藥產(chǎn)業(yè)技術(shù)創(chuàng)新聯(lián)盟致力于建立產(chǎn)業(yè)技術(shù)發(fā)展信息交流平臺,,收集了解產(chǎn)業(yè)技術(shù)創(chuàng)新過程中的需求,,為聯(lián)盟成員單位提供技術(shù),、產(chǎn)品,、人力資源和信息、咨詢,、培訓(xùn)等綜合服務(wù),;受企業(yè)委托,對科技成果的技術(shù)水平和產(chǎn)業(yè)化前景進行評估,;定期舉辦獸藥行業(yè)技術(shù)創(chuàng)新論壇,,加強成員單位間的信息交流,提出切實建議,,凝聚產(chǎn)業(yè)共識,,積極為國家政策獻言獻策,引導(dǎo)行業(yè)健康發(fā)展,。為此,,聯(lián)盟微信公眾號設(shè)立《新技術(shù)&研究進展》欄目,收集,、發(fā)布獸藥產(chǎn)業(yè)相關(guān)技術(shù)創(chuàng)新及研究進展,。
為探討優(yōu)化我國獸用生物制品支原體檢驗方法的可能性,從支原體檢驗方法,、培養(yǎng)基種類及培養(yǎng)條件,、培養(yǎng)基質(zhì)量控制和檢驗操作方法四個方面,對中國,、美國和歐盟獸用生物制品支原體檢驗方法進行系統(tǒng)比較,,分析不同方法之間的差異及優(yōu)劣,。結(jié)果發(fā)現(xiàn),與美國《聯(lián)邦法規(guī)》第九卷及《歐洲藥典》相比《中國獸藥典》支原體檢驗方法有培養(yǎng)基種類及配方成分全面等方面的優(yōu)勢,,但在培養(yǎng)基質(zhì)量控制方法,、檢驗過程控制、檢驗標(biāo)準(zhǔn)制定等方面還存在不足,。正視這些差距與不足,,提出改進和驗證的方向,可為我國獸用生物制品支原體檢驗的優(yōu)化提供參考,。基金項目:獸藥行業(yè)公益性重點專項(GY202007)作者簡介:馬欣,,助理研究員,碩士,,從事細菌類生物制品的檢測及相關(guān)科研工作,。支原體是獸用生物制品中較常見的污染物,,其主要來源于環(huán)境,、污染的種毒、細胞或雞胚等,。支原體污染會對獸用生物制品生產(chǎn)的一致性及產(chǎn)品的安全性產(chǎn)生重大影響,。高效、敏感,、準(zhǔn)確的檢驗方法可以提高支原體污染的檢出效率,,降低污染擴散風(fēng)險,保障畜牧業(yè)健康發(fā)展,。不同國家對獸用生物制品支原體檢驗依據(jù)各異,,中國獸用生物制品支原體檢驗依據(jù)現(xiàn)行《中國獸藥典》2020版第三部附錄3308;美國獸用生物制品支原體檢驗依據(jù)現(xiàn)行《美國聯(lián)邦法規(guī)》第九卷(以下簡稱9CFR)113.28,;歐盟國家獸用生物制品支原體檢驗依據(jù)現(xiàn)行《歐洲藥典》10.0版(EP10.0)2.6.7章節(jié),。本文對美國、歐盟和我國獸用生物制品支原體檢驗方法進行對比,,從支原體檢驗方法,、培養(yǎng)基種類、培養(yǎng)基質(zhì)量控制和操作方法等四個方面分析不同方法之間的差異及優(yōu)勢,,以期為國內(nèi)現(xiàn)有支原體檢驗方法的優(yōu)化提供新思路,。三部法典所規(guī)定的支原體檢驗方法存在一定的差異,《中國獸藥典》和9CFR中支原體檢驗方法為培養(yǎng)法,,《歐洲藥典》 中支原體的檢驗方法有三種,,分別為培養(yǎng)法、指示細胞培養(yǎng)法和核酸擴增檢測法,?!?/span>歐洲藥典》 規(guī)定對種子細胞庫、工作細胞庫,、病毒種子批或者對照細胞進行支原體檢驗時,,需要同時使用培養(yǎng)法和指示細胞培養(yǎng)法;在對病毒原液,、半成品和成品進行支原體檢驗時,,需用培養(yǎng)法;如需要篩選培養(yǎng)基可以選用指示細胞培養(yǎng)法,;核酸擴增檢測法則需通過驗證試驗后方可對前兩種方法進行替代,。培養(yǎng)法是支原體檢驗的經(jīng)典方法。雖然在上述三部法典中培養(yǎng)法在細節(jié)上不盡相同,,但大致步驟均為用液體培養(yǎng)基培養(yǎng)待檢樣品,,每隔一段時間進行固體培養(yǎng)基和液體培養(yǎng)基移植,最后根據(jù)固體平板上菌落生長情況判定結(jié)果,。該方法根據(jù)支原體的生長特性通過長時間培養(yǎng)和多次移植,,可檢出能在培養(yǎng)基中生長的各類支原體,具有較高的普適性和靈敏度,。但是培養(yǎng)法需要28~29日的檢驗周期,,對于一些需要快速通行的中間產(chǎn)物或半成品檢驗具有一定的局限性。由于培養(yǎng)法是《中國獸藥典》和9CFR中支原體檢驗的唯一方法,,因此本文將重點比較三部法典中支原體檢驗培養(yǎng)法的差別,。指示細胞培養(yǎng)法是將檢品接種于指示細胞中培養(yǎng),然后用特異熒光染料染色,,在顯微鏡下觀察是否有支原體DNA著色,。該方法雖然在《中國獸藥典》和9CFR中未提及,但是在醫(yī)藥領(lǐng)域已是成熟的檢驗方法,,其作為第二種支原體檢驗法被收錄在《中國藥典》,、《歐洲藥典》和《美國藥典》 中。指示細胞培養(yǎng)法完整檢驗時間在14日左右,,檢驗周期方面比培養(yǎng)法有優(yōu)勢,,但由于該方法需要將檢品與指示細胞共同培養(yǎng),更適合檢驗細胞或培養(yǎng)基中支原體污染情況,,若檢品為可導(dǎo)致指示細胞病變的病毒樣本,,則需要用特異性抗血清先進行病毒中和,因此不適用于缺少有效中和抗體的高滴度病毒樣本,。支原體核酸擴增檢測法(NAT)是用支原體特異性引物對檢品中提取的核酸進行擴增,,通過檢測特定核酸序列來判定檢品是否存在支原體污染。在《歐洲藥典》中NAT法做為第三種支原體檢測法可供選擇,,藥典中未提供具體方法,,根據(jù)驗證指南對使用方法進行驗證試驗,,若結(jié)果符合要求可作為培養(yǎng)法或指示細胞培養(yǎng)法的替代方法。9CFR中未提及NAT法,,但是美國農(nóng)業(yè)部獸醫(yī)生物制品中心發(fā)布的檢驗規(guī)程中有一項為聚合酶鏈?zhǔn)椒磻?yīng)檢測支原體污染,,該規(guī)程中提供了具體的檢測方法,并表明此方法可與9CFR中的培養(yǎng)法結(jié)合或獨立使用,。NAT法具有檢驗周期短,、操作簡單、靈敏度高的特點,,但是由于該方法檢測出的是特定核酸序列,,并非活的支原體,檢驗結(jié)果可能出現(xiàn)假陽性,。《中國獸藥典》,、9CFR及《歐洲藥典》中用于支原體檢驗的培養(yǎng)基各不相同?!?/span>中國獸藥典》和9CFR中用于支原體檢驗的培養(yǎng)基各有三種和一種,,由于《歐洲藥典》同時應(yīng)用于醫(yī)藥和獸藥兩個領(lǐng)域,故支原體檢驗用培養(yǎng)基種類較多,,其中涉及獸藥檢驗的有三種,。三部法典中培養(yǎng)基種類及用途詳見表1。
《中國獸藥典》和《歐洲藥典》針對禽源支原體和非禽源支原體檢驗均有相應(yīng)的培養(yǎng)基,,與 9CFR只有一種通用培養(yǎng)基相比,,這兩部法典的培養(yǎng)基種類更豐富。另外,,考慮到對血清進行支原體檢驗時檢品本身是一種培養(yǎng)基中添加的營養(yǎng)成分,,《中國獸藥典》設(shè)置了不添加血清的支原體培養(yǎng)基,更加全面地滿足不同檢品的需求,。由于支原體基因組分子量小,,生物合成能力有限,需從外界攝取大量能源物質(zhì),,導(dǎo)致支原體對于生長條件要求較為苛刻,,需要在營養(yǎng)物質(zhì)豐富的培養(yǎng)基中才能生長。三部法典中培養(yǎng)基雖然在種類和數(shù)量方面有差異,,但各培養(yǎng)基中營養(yǎng)成分類別大致相同,。不同之處僅區(qū)別在是否添加指示劑、緩沖劑,、輔酶,、脫氧核糖核酸等物質(zhì)。具體添加成分見表2,固體培養(yǎng)基成分與配套液體培養(yǎng)基除增加瓊脂外基本一致,。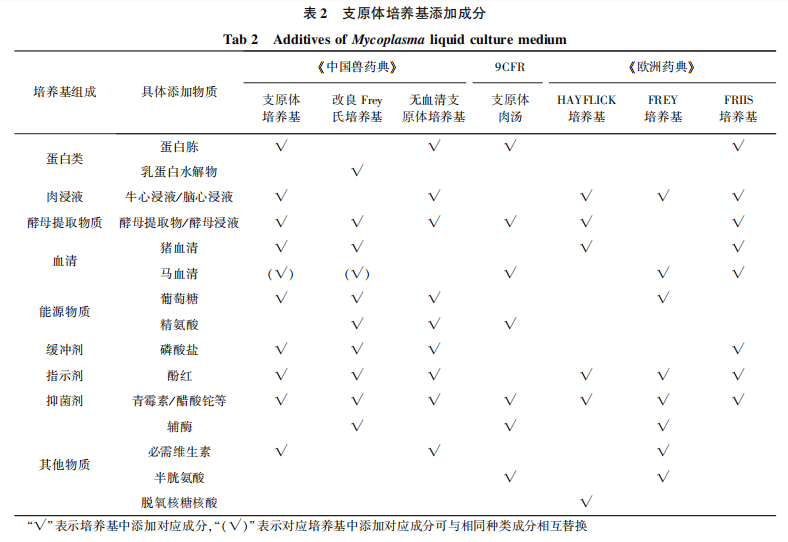
在培養(yǎng)基配方方面,,三部法典的培養(yǎng)基中均含有對應(yīng)適宜支原體生長所需的營養(yǎng)物質(zhì),如培養(yǎng)滑液囊支原體需在培養(yǎng)基中添加輔酶成分,,在《中國獸藥典》中用于禽源支原體檢驗的改良Frey氏培養(yǎng)基和《歐洲藥典》 用于滑液囊支原體檢驗的FREY培養(yǎng)基中均有該成分,,雖然9CFR只有一種支原體肉湯培養(yǎng)基,,但也添加了輔酶成分,,可以保證滿足各類支原體的生長需求。9CFR的支原體肉湯培養(yǎng)基,、《 歐洲藥典》 的HAYFLICK培養(yǎng)基和FREY培養(yǎng)基中未添加有緩沖作用的無機鹽,,發(fā)酵型支原體在生長過程中會分解培養(yǎng)基中的糖類物質(zhì)而產(chǎn)酸,然而支原體對于pH變化敏感,,pH低于7.0的環(huán)境會抑制生長或?qū)е滤劳?/span>,,因此支原體培養(yǎng)基應(yīng)具有良好的緩沖能力,添加有緩沖作用的無機鹽是有必要的,。需要注意的是支原體對滲透壓比較敏感,,緩沖物質(zhì)濃度應(yīng)保持在一定限度。支原體肉湯培養(yǎng)基中未添加指示劑,,可通過混濁度來辨別支原體是否生長,,但是添加指示劑(通常為酚紅)使得培養(yǎng)基的pH變化更容易被發(fā)現(xiàn),有更強的提示作用,。綜上,,《中國獸藥典》中三種支原體培養(yǎng)基組成成分較為全面,可滿足相應(yīng)支原體的生長需求,。通常情況下生物制品中污染支原體的含量比較少,,因此培養(yǎng)基的質(zhì)量優(yōu)劣是能否檢驗出支原體污染的關(guān)鍵,培養(yǎng)基質(zhì)量控制是為支原體檢驗保駕護航的重要步驟,?!?/span>中國獸藥典》和《歐洲藥典》 中均規(guī)定了支原體檢驗用培養(yǎng)基質(zhì)量控制方法,9CFR中沒有相應(yīng)規(guī)定,,但是美國獸醫(yī)生物制品補充檢驗方法(SAM)第910條支原體污染檢測補充檢驗方法中,,規(guī)定用促生長能力對培養(yǎng)基進行質(zhì)量控制。三部法典的質(zhì)量控制方法存在差異,,具體內(nèi)容比較見表 3,。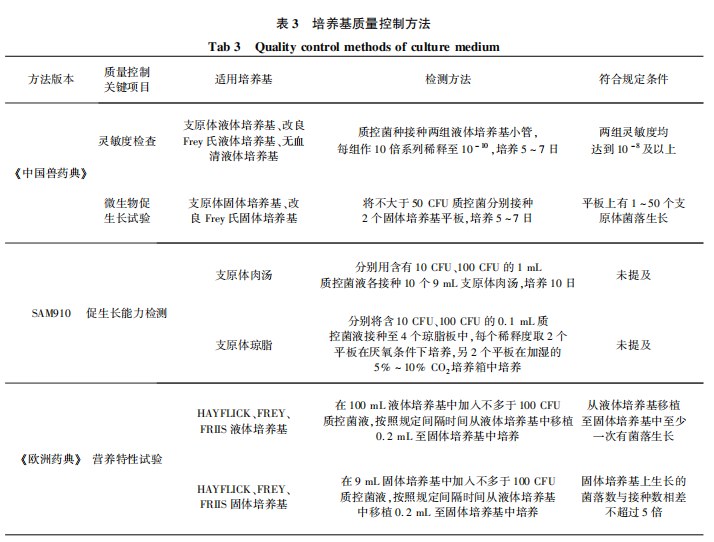
3.2 培養(yǎng)基質(zhì)量控制用菌種 三部法典關(guān)于培養(yǎng)基質(zhì)量控制用菌種也有所不同?!?/span>中國獸藥典》 和9CFR中各有2種菌株用于支原體檢驗培養(yǎng)基質(zhì)控,,菌株種類及對應(yīng)質(zhì)控培養(yǎng)基類型見表4。《歐洲藥典》中涉及獸用生物制品支原體培養(yǎng)基的質(zhì)控菌株有5種,,未明確規(guī)定不同培養(yǎng)基對質(zhì)控菌種的選擇,,但規(guī)定質(zhì)控菌種繼代次數(shù)不能超過15代。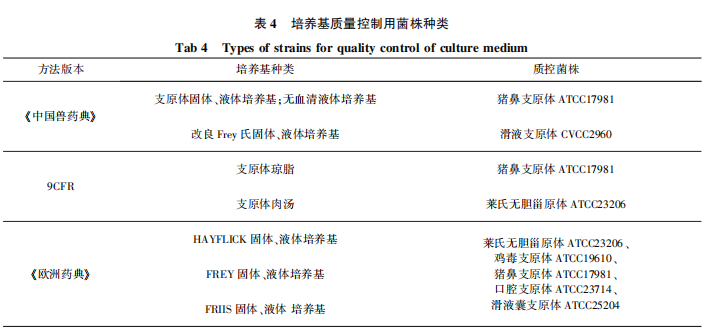
在培養(yǎng)基質(zhì)量控制方面,,《中國獸藥典》和《歐洲藥典》在液體培養(yǎng)基質(zhì)量控制上檢驗方法雖不相同,,但對于液體培養(yǎng)基靈敏度要求相似。需要注意的是,,《中國獸藥典》中所采用的觀察液體培養(yǎng)顏色變化是間接指標(biāo),,易受諸多因素干擾,用該方法進行培養(yǎng)基質(zhì)控其結(jié)果的準(zhǔn)確與否有待深入探討,。在固體培養(yǎng)基的質(zhì)量控制中,,《中國獸藥典》微生物促生長試驗要求將不大于50CFU質(zhì)控菌株接種平板,菌落數(shù)為1~50CFU判定合格,,《歐洲藥典》營養(yǎng)代謝特性試驗規(guī)定接種不多于100CFU質(zhì)控菌株,,要求菌落數(shù)與接種數(shù)量相差不超過5倍,菌落生長數(shù)量會因為培養(yǎng)基營養(yǎng)水平不同根據(jù)接種菌量在一定范圍內(nèi)浮動,,因此對于菌落生長數(shù)量的上限及下限要求對培養(yǎng)基質(zhì)量控制至關(guān)重要,,《中國獸藥典》中對于菌落生長數(shù)量的要求為一個固定的范圍,未體現(xiàn)與接種菌量的關(guān)系,。另外,,《歐洲藥典》對質(zhì)控菌種的傳代次數(shù)做出了規(guī)定(不超過15代),《中國獸藥典》在2010年版時要求質(zhì)控菌株傳代不超過5代,,在2015年版和現(xiàn)行2020年版中均無相應(yīng)要求,。支原體隨著傳代次數(shù)的增多,其生長特性會發(fā)生相應(yīng)的變化,,因此對于質(zhì)控菌株的代次限制可對培養(yǎng)基質(zhì)量控制的可靠性提供保障,,質(zhì)控菌株的最高代次還需根據(jù)進一步試驗數(shù)據(jù)結(jié)果進行設(shè)定。三部法典規(guī)定的支原體檢驗操作方法存在差異,,在取樣量,、培養(yǎng)溫度、移植及培養(yǎng)觀察時間,、移植取樣量,、陽性對照接種量和對照成立條件上均有差別。支原體檢驗培養(yǎng)法具體差異比較見表5,。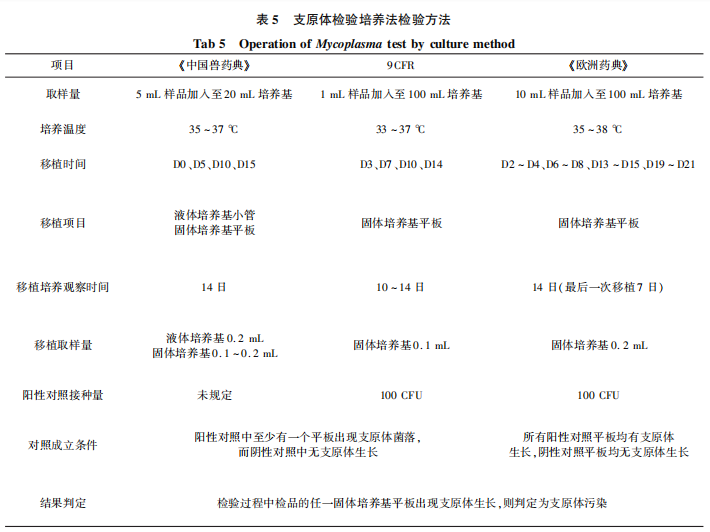
在支原體檢驗操作方法方面,,《中國獸藥典》中明確規(guī)定取5瓶樣品進行檢驗,另兩部法典未對取樣方法進行說明,。在取樣量上,,《中國獸藥典》為5mL樣品接種至20mL 培養(yǎng)基中,,為1:4接種,在三部法典中接種濃度最高(9CFR 為1:100,,《歐洲藥典》為1:10),,接種的檢品在一定范圍內(nèi)占比越大,檢出支原體污染的概率就越高,,由此可見《中國獸藥典》支原體檢驗在接種量方面要求最為嚴(yán)格,。值得一提的是,《歐洲藥典》在進行檢驗之前還會對給定產(chǎn)品進行抑制物質(zhì)檢測,,通過對比培養(yǎng)基中添加檢品和不添加檢品的支原體菌株生長情況,,檢測其是否含有抑制物質(zhì)。若結(jié)果含有抑制物質(zhì),,則需進行中和或者經(jīng)過加大培養(yǎng)基體積進行稀釋后再進行抑制物質(zhì)檢查,。該步驟能夠避免一些檢品中因含有抑制支原體生長物質(zhì)導(dǎo)致支原體檢驗結(jié)果出現(xiàn)假陰性的問題,從而提高檢驗結(jié)果的準(zhǔn)確性,。《中國獸藥典》在每次固體培養(yǎng)基平皿移植的同時也做液體培養(yǎng)基小管的移植,此步驟是其他法典中沒有的,。雖然在最后結(jié)果判定中是以固體平板為準(zhǔn),,但是在實際檢驗過程中,液體小管的顏色變化對該次移植平皿中是否有支原體生長起了很好的提示作用,,這一步驟是有必要的,。《歐洲藥典》 和SAM910均明確規(guī)定陽性對照接種菌量為不大于100CFU,,而《中國獸藥典》 沒有相應(yīng)要求,,規(guī)定陽性對照接種量可以更好地反應(yīng)本次移植培養(yǎng)基的質(zhì)量情況,及時發(fā)現(xiàn)培養(yǎng)基質(zhì)量問題,,避免漏檢情況出現(xiàn),。在試驗成立條件方面,由于9CFR中陽性對照設(shè)定需接種至液體培養(yǎng)基與檢品同時培養(yǎng),,每次移植取陽性對照培養(yǎng)物接種平板,,有可能出現(xiàn)在第二次、第三次或第四次移植時由于培養(yǎng)基中營養(yǎng)成分耗盡或pH值變化較大,,使得陽性對照培養(yǎng)瓶中已無活支原體的情況,,因此,9CFR規(guī)定陽性對照中至少有一個平板出現(xiàn)支原體菌落即為試驗成立,。《中國獸藥典》與《歐洲藥典》每次移植時設(shè)定的陽性對照均為活的陽性對照菌株且《歐洲藥典》要求每次接種菌量為100CFU,,不存在類似9CFR在移植時無活的支原體的情況。但是《中國獸藥典》在結(jié)果判定時仍規(guī)定為陽性對照中至少有一個平板出現(xiàn)支原體菌落即為試驗成立,,標(biāo)準(zhǔn)較低,,相比之下《歐洲藥典》中要求的所有陽性對照平板均有支原體生長為試驗成立,能更好地確保每次移植試驗結(jié)果的可靠性。支原體污染是獸用生物制品外源因子污染中最常見的問題,,可靠的檢驗方法可以從源頭減少支原體污染帶來的安全隱患,。在《 中國獸藥典》、9CFR和《歐洲藥典》 所涵蓋的三種支原體檢驗方法中,,培養(yǎng)法無論是在適用性還是結(jié)果的準(zhǔn)確性方面均比其他兩種方法有優(yōu)勢,,目前仍是獸用生物制品支原體檢驗的金標(biāo)準(zhǔn)。NAT法具有高效,、敏感的特點,,彌補了培養(yǎng)法檢驗周期長的缺陷,是美國和歐盟均認可的支原體檢測方法,,在國內(nèi)也有很多關(guān)于支原體檢驗PCR方法研究的報道,。然而《中國藥典》及《中國獸藥典》均未收錄該方法,表明國內(nèi)對應(yīng)用NAT方法持謹慎態(tài)度,。究其原因除了因為該方法檢出結(jié)果有假陽性的風(fēng)險外,,另一方面,若以此方法出具正式檢驗結(jié)果則對目的基因及引物序列有較高要求,,既要有較強的特異性,,確保不會對同源性強的細菌造成誤檢;又要具備較好的普適性,,盡可能適用生物制品中常見的各類支原體,,以免發(fā)生漏檢。同時滿足這兩點要求對于目的基因以及對應(yīng)引物的篩選可能有一定的難度,。由于NAT法本身存在的這些特性,,《歐洲藥典》和《美國藥典》并未將其作為官方方法與其他兩種方法同樣直接使用,而是要求需進行驗證后方可使用,,《歐洲藥典》NAT法驗證指南中對使用方法的特異性,、最低檢測限及耐用性提出了具體的要求。因此,,若使用NAT法檢測支原體污染或作為培養(yǎng)法,、指示細胞培養(yǎng)法的替代方法,需對使用方法進行充分驗證,,可將該指南驗證方法作為參考或進行優(yōu)化,,盡可能提高檢驗方法的特異性和適用性,避免誤檢和漏檢的情況發(fā)生,。在培養(yǎng)法方面,,《中國獸藥典》與9CFR和《歐洲藥典》相比培養(yǎng)基種類及配方成分更全面,盡可能滿足不同檢品的需求,;檢驗時檢品接種量最大,,對檢品的要求更為嚴(yán)格,,這些是我們的優(yōu)勢。但是通過比較也發(fā)現(xiàn)《中國獸藥典》在培養(yǎng)基質(zhì)量控制,、檢驗操作及檢驗標(biāo)準(zhǔn)方面存在一些不足,,在此提出一些改進和驗證的思路,作為未來優(yōu)化方向的參考,。①在進行培養(yǎng)基質(zhì)量控制時,,明確質(zhì)控菌種最高使用代次;②液體培養(yǎng)基的靈敏度檢查法最終判定標(biāo)準(zhǔn)修改為以固體平皿上有菌落生長準(zhǔn),;③固體培養(yǎng)基微生物促生長試驗菌落生長數(shù)量根據(jù)接種數(shù)量進行定值,;④在每次檢驗操作時,明確陽性對照接種數(shù)量,;⑤ 適當(dāng)提高檢驗時陽性對照成立標(biāo)準(zhǔn),。通過對《中國獸藥典》、9CFR和《歐洲藥典》進行系統(tǒng)比較,,發(fā)現(xiàn)我國獸用生物制品支原體檢驗方法與歐美國家存在較大差異,,既有優(yōu)勢也有不足。今后可從豐富支原體檢驗方法,、優(yōu)化培養(yǎng)基質(zhì)量控制方法,、規(guī)范檢驗過程控制,完善檢驗標(biāo)準(zhǔn)等方面進行改進和驗證,,以提高支原體檢驗的時效性和檢測結(jié)果的準(zhǔn)確性。








